Neue Richtlinien zur Blutgruppenbestimmung und Bluttransfusion
(Hämotherapie) 1996
Rhesus-D-Bestimmung beim Transfusionsempfänger
Willy A. Flegel,
Hinnak Northoff und Franz F.
Wagner
Dieser Hypertext wurde in Anlehnung an die Veröffentlichung in
der MTA Zeitschrift 13(1998)83,
Heft 2 vom Februar 1998 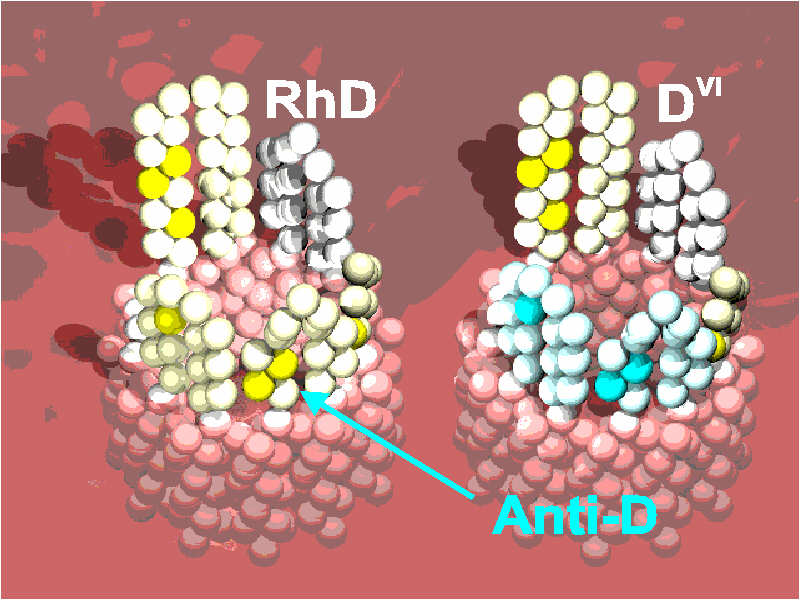 gestaltet.
Die Autoren bedanken sich beim Umschau Zeitschriftenverlag
und der Chefredakteurin Dr. S. Päuser
für die freundliche Genehmigung zur elektronischen Wiedergabe des
Zeitschriftenbeitrags. Auszüge aus dem zugrundeliegenden Manuskript
wurden 1997 auch als Verlautbarung des Berufsverbandes Deutscher Transfusionsmediziner
unter dem Titel Stand der Rhesus-D Bestimmung beim Transfusionsempfänger
veröffentlicht.
gestaltet.
Die Autoren bedanken sich beim Umschau Zeitschriftenverlag
und der Chefredakteurin Dr. S. Päuser
für die freundliche Genehmigung zur elektronischen Wiedergabe des
Zeitschriftenbeitrags. Auszüge aus dem zugrundeliegenden Manuskript
wurden 1997 auch als Verlautbarung des Berufsverbandes Deutscher Transfusionsmediziner
unter dem Titel Stand der Rhesus-D Bestimmung beim Transfusionsempfänger
veröffentlicht.
Inhaltsübersicht
Fakten & Thesen
-
zwei monoklonale anti-D vom IgM-Typ, die die Kategorie DVI
nicht erfassen
-
auf unterschiedliche Klonbezeichnungen achten
-
keinen Antiglobulintest durchführen (bei Untersuchung
von Transfusionsempfängern, Schwangeren und Neugeborenen)
-
für Blutgruppenbestimmung sensitive Techniken einsetzen
(nicht Objektträger)
-
Eigenkontrolle muß immer durchgeführt werden und
einwandfrei negativ sein.
-
Bei übereinstimmend positiven Ergebnissen genügen
auch schwach positive Reaktionen (zum Beispiel ++) für einen Befund
Rh pos.
-
Diskrepante oder fraglich positive Ergebnisse treten nur
selten auf (< 1:1.000).
-
Meist ist es wirtschaftlich, wenn die seltenen fraglich positiven
Ergebnisse von einem Referenzlabor geklärt werden.
-
Eine gezielte Diagnostik für partielle Rhesus-D-Antigene,
zum Beispiel Rhesus-D-Kategorien, ist beim Transfusionsempfänger nicht
erforderlich.
-
rein polyklonale Antiseren (humanes anti-D ohne monoklonale
Antikörper) für die patientenbezogene Rhesus-D-Bestimmung nicht
mehr verwenden
-
anti-D Alloantikörper bei Rhesus positiven Patienten
wissenschaftlich untersuchen lassen (Online-Informationen
und Meldebogen)
Einleitung
Die Neufassung der Richtlinien zur Blutgruppenbestimmung
und Bluttransfusion (Hämotherapie) [1] bringt wesentliche
Vereinfachungen bei der AB0- und Rhesus-Blutgruppenbestimmung. Dies wurde
unter anderem erreicht durch den Verzicht auf polyklonale Antiseren und
den Einsatz monoklonaler Antikörper in der patientenbezogenen Rhesus-D-Diagnostik.
Für das Rhesus-D-Antigen unterscheidet sich zukünftig die serologische
Diagnostik zwischen Patienten (alle potentiellen Transfusionsempfänger)
und Blutspendern - eine Trennung, die im Ausland seit langem üblich
ist. Die in den Richtlinien festgelegte Rhesus-D-Diagnostik optimiert den
therapeutischen Vorteil für den Patienten. Sie ist wirksam, gefahrlos
und kosteneffizienter als das bisher gültige Vorgehen. Wir erwarten,
daß sich die neue Rhesus-D-Bestimmung gerade wegen der vereinfachten
Diagnostik sehr schnell in der Praxis der Routinelabors durchsetzt.
Klinische Bedeutung partieller
Rhesus-D-Antigene
Bei partiellen Rhesus-D-Antigenen, wie zum Beispiel D
Kategorien, liegt ein strukturell verändertes Rhesus-D-Protein vor.
Manche Träger von partiellen Rhesus-D-Antigenen bilden deswegen nach
Rhesus positiven Transfusionen anti-D Alloantikörper. Diese anti-D
Alloantikörper sind gegen die Anteile des vollständigen Antigen
D gerichtet, die der Träger des entsprechenden partiellen Rhesus-D-Antigens
nicht besitzt (siehe unten). Partielle Rhesus-D-Antigene
sind sehr viel häufiger als bisher vermutet (Tabelle 1).
Tabelle 1. Häufigkeit von partiellen Rhesus-D-Antigenen
(RhD) in Baden-Württemberg und repräsentative RhD Antigendichten.
(Nach [2], [6], [18]
und [8]. Mittelwerte der beobachteten Häufigkeit
unter > 64.000 Blutspendern. n. d. - nicht durchgeführt.)

D Kategorie VII ist das häufigste partielle Rhesus-D-Antigen
mit einer Phänotyp-Frequenz von 1:900 [6], ohne daß
das Rhesus-D-Antigen wesentlich abgeschwächt ist (kein Du) [7,
8]. Schon in der bisherigen Praxis sind Patienten mit
D Kategorie VII Rhesus-D-positiv transfundiert worden [2].
Trotzdem wurden in Deutschland praktisch keine Immunisierungen beobachtet.
Ähnliches gilt für DIV und DII [7, 8,
9]. Patienten mit solchen partiellen Rhesus-D-Antigenen
einschließlich D Kategorien brauchen nicht Rhesus negativ versorgt
zu werden [2, 10]. Im Gegensatz hierzu
bilden Patienten mit einer D Kategorie VI verhältnismäßig
häufig einen anti-D Alloantikörper und müssen nach den Richtlinien
deswegen Rhesus negativ transfundiert werden. Nach jetzigem Kenntnisstand
ist die D Kategorie VI mit einer Phänotyp-Frequenz von etwa 1:6.000
in Deutschland das häufigste klinisch relevante partielle Rhesus-D-Antigen
und wurde früher als Du typisiert beziehungsweise Rhesus negativ
transfundiert. Immerhin circa 6 % aller Du waren D Kategorie VI [2].
Deswegen wurde die D Kategorie VI bei der Rhesus-D-Bestimmung der neuen
Richtlinien [1] und in den Transfusionsempfehlungen
der Leitlinien [11] berücksichtigt und eine Rhesus
negative Transfusion vorgeschrieben.
Richtlinien-konforme
Rhesus-D-Bestimmung
Ein seit Ende 1996 gültiges diagnostisches Vorgehen
bei der serologischen Rhesus-D-Bestimmung ist in Tabelle 2 zusammengefaßt.
Tabelle 2. Diagnostisches Vorgehen zur Rhesus-D-Bestimmung
bei Patienten (z. B. potentielle Transfusionsempfänger, Schwangere,
Neugeborene) und Empfehlungen für die Transfusionstherapie.

Nach Wagner et al. [2] und Tabelle 3
in [3]. Entspricht den Richtlinien zur Blutgruppenbestimmung
und Bluttransfusion (Hämotherapie) [1] und den Leitlinien
zur Therapie mit Blutkomponenten und Plasmaderivaten [11]
1 - Beide anti-D sollen monoklonale Antikörper vom
IgM-Typ sein, die die D Kategorie VI nicht erfassen. Technik nach Angaben
des Herstellers (kein Antiglobulintest). 2 - auch bei Du als Vorbefund,
3 - oder fraglich positiver Befund
Der Antiglobulintest soll bei der patientenbezogenen Rhesus-D-Bestimmung
in der Regel nicht mehr eingesetzt werden. Wir halten es für sinnvoll,
daß Labore ohne spezialisierte Immunhämatologie von dem in Tabelle
1 dargestellten diagnostischen Vorgehen nicht abweichen und eine weitere
Abklärung zum Beispiel mittels Antiglobulintest an ein Referenzlabor
weiterleiten. Es wird nicht mehr zwischen D positiv und Du unterschieden.
Der Begriff Du wird nicht mehr benutzt. Eine gezielte Diagnostik für
schwache oder partielle Rhesus-D-Antigene, zum Beispiel D Kategorie VI,
braucht beim Patienten nicht zu erfolgen. Die dargestellte Rhesus-D-Diagnostik
gilt auch für Patienten, bei denen eine Eigenblutabnahme und -transfusion
durchgeführt wird, und für Eigenblutpräparate.
Anti-D Testreagenzien und Technik
Die Rhesus-D-Bestimmung erfolgt mit zwei anti-D-Testreagenzien
(Tabelle 2). Die Anwendung von zwei monoklonalen Antikörpern vom IgM-Typ
wird empfohlen. Beide monoklonale Antikörper dürfen die D Kategorie
VI nicht erfassen und müssen unterschiedliche Klonbezeichnungen aufweisen
(nach Angaben des Herstellers im Beipackzettel). Reagenzien mit jeweils
einem isolierten monoklonalen IgM anti-D sind vorzuziehen. Geeignete IgM
anti-D, die mit polyklonalem anti-D oder monoklonalem IgG anti-D gemischt
sind, können verwendet werden. Bei diesen gemischten Seren sollte
ebenfalls kein Antiglobulintest durchgeführt werden, da sonst Patienten
mit D Kategorie VI als Rhesus positiv typisiert würden. Das neue Vorgehen
nutzt die sehr hohe Sensitivität monoklonaler IgM anti-D gegenüber
schwach ausgeprägten Antigen D (früher Du) aus. Rein polyklonale
Antiseren (humanes anti-D ohne Beimischung von geeigneten monoklonalen
Antikörpern) sollten nicht mehr eingesetzt werden, da sie aufgrund
ihrer ohne Antiglobulintest geringen Sensitivität für schwach
ausgeprägtes Antigen D bei dem in Tabelle 1 vorgeschlagenen Vorgehen
zu einer unnötig hohen Rate falsch-negativer Befunde führen würden.
Eigenkontrolle
Eine Eigenkontrolle (Prüfung auf Autoagglutination)
zum Beispiel mit Rhesuskontrollserum muß wie bisher bei jeder Rhesus-D-Blutgruppenbestimmung
durchgeführt werden und eindeutig negativ sein. Da auch schwach positive
Reaktionen zur Rhesus-D-Diagnostik herangezogen werden, kommt dieser Eigenkontrolle
große Bedeutung zu. Insbesondere können durch die Eigenkontrolle
falsch positive Reaktionen infolge technischer Probleme (zum Beispiel Geldrollenphänomen
oder positiver direkter Antiglobulintest) erkannt und eine Rhesus-D-Fehlbestimmung
vermieden werden. Eine Eigenkontrolle, die im Rahmen eines Antikörpersuchtestes
durchgeführt wird, kann auch als Eigenkontrolle der Rhesus-D-Bestimmung
herangezogen werden, vorausgesetzt die Untersuchungen werden zusammen angesetzt
und beurteilt. Entsprechend den Richtlinien zur Qualitätssicherung
[4] sind wie bisher regelmäßig (mindestens
1 mal pro Woche) positive und negative Kontrollen mit D-positiven und D-negativen
Testerythrozyten mitzuführen.
Ergebnisbeurteilung
Es ist vorteilhaft, sensitive Techniken einzusetzen (Röhrchen-
oder Gelmatrix-Techniken). Die Rhesus-D-Bestimmung auf dem Objektträger
ist vergleichsweise weniger sensitiv und als Verfahren der Rhesus-D-Blutgruppenbestimmung
nicht zu empfehlen. Der Objektträgertest kann aber noch für eine
Inhaltskontrolle benutzt werden.
Für ein positives Ergebnis genügt eine übereinstimmend
+ (einfach positive) bis ++ (zweifach positive) Reaktion in den beiden
Testansätzen der Tabelle 1 entsprechend den üblichen Kriterien
der blutgruppenserologischen Diagnostik. Bei diskrepanten oder schwach
(fraglich) positiven Ergebnissen in den Testansätzen ist eine Klärung
notwendig. Ein solches Ergebnis ist - ausreichend sensitive Technik vorausgesetzt
- nur bei 1 unter 1.000 Patienten oder seltener zu erwarten. Eine Abklärung
kann von dem zuständigen blutgruppenserologischen Referenzlabor, das
über entsprechende Erfahrung verfügt, mit geeigneten Testreagenzien
zum Beispiel im indirekten Antiglobulintest durchgeführt werden. In
Abhängigkeit vom Ergebnis wird der Befund Antigen D schwach ausgeprägt
(= weak D) [5] gestellt und im Einzelfall eine Empfehlung
zur Rhesus-D-positiven oder Rhesus-D-negativen Transfusion gegeben werden.
Meist ist es für Routinelabore auch ökonomisch
günstiger, die seltenen fraglich positiven Ergebnisse von einem Referenzlabor
klären zu lassen, anstatt die erforderlichen Antiseren und den aktuellen
Wissensstand für eine weitergehende Beurteilung schwach ausgeprägter
Rhesus-D-Antigene im eigenen Labor vorzuhalten. Ein solches Vorgehen ist
Richlinien-konform. Eine sichere Differenzierung von schwach ausgeprägten
Antigen D und klinisch relevantem partiellem Antigen D, unter anderem D
Kategorie VI, erfordert den Einsatz unterschiedlicher monoklonaler anti-D
zum Beispiel vom IgG-Typ, weil auch ein partielles Antigen D im Antiglobulintest
mit polyklonalen Antiseren stark positiv reagiert.
Transfusion, Blutgruppendokumente
und anti-D-Prophylaxe
Für ein abgeschwächtes Antigen D kann der in
den Richtlinien neu eingeführte Begriff Dweak verwendet werden,
der in der internationalen Literatur ursprünglich als weak D definiert
wurde [5]. Eine exakte Abgrenzung zwischen normalem Antigen
D und Dweak ist nicht definiert. Da ein abgeschwächtes Antigen D
bei Patienten wie bei Blutspendern als Rh pos. behandelt wird, hat der
Begriff Dweak eine untergeordnete Bedeutung.
Viele Blutproben mit schwachem Antigen D, die früher
als Du eingestuft wurden, reagieren in beiden Testansätzen positiv
(siehe Tabelle 2) und werden deswegen als Rhesus-D-positiv beurteilt. Diese
Patienten werden Rhesus-D-positiv transfundiert und erhalten keine anti-D-Prophylaxe.
In neuen Blutgruppenausweisen muß Rhesus-D-positiv vermerkt werden.
Bei Patienten mit bekanntem Du sollte die Rhesus-D-Bestimmung wie bei
einem Patienten ohne Vorbefund durchgeführt werden.
Alle Blutproben mit D Kategorie VI und einzelne früher
als Du befundete Blutproben reagieren in beiden Testansätzen negativ
und werden als Rhesus-D-negativ behandelt. Diese Patienten werden demzufolge
mit Rhesus-D-negativen Erythrozytenpräparaten transfundiert und erhalten,
wenn indiziert, eine anti-D-Prophylaxe. In Blutgruppenausweisen für
diese Patienten kann Rhesus-D-negativ vermerkt werden. Man kann erwägen,
grundsätzlich auf eine anti-D-Prophylaxe zu verzichten, wenn der sichere
Kindsvater Rhesus-D-negativ ist.
Proben mit bekannten Du, die in der Rhesus-D-Bestimmung
nach den aktuellen Richtlinien negativ reagieren, sind verdächtig
für partielle Rhesus-D-Antigene und können in einem Referenzlabor
abgeklärt werden. Wird bei einem Rhesus positiven Patienten die Bildung
eines anti D Alloantikörpers beobachtet, so ist dies von erheblichem
praktischem und wissenschaftlichem Interesse. Im Sinne einer Qualitätssicherung
der medizinischen Diagnostik sollten solche seltenen Ereignisse unbedingt
von einem spezialisierten Labor verifiziert werden, um ihre Bedeutung für
die Weiterentwicklung der Diagnostik einzustufen. Eine vollständige
Erfassung solcher Proben wird vom der Sektion 5 der Deutschen Gesellschaft
für Transfusionsmedizin und Immunhämatologie angestrebt (Rhesus
Immunisierungsregister [RIR] der DGTI: Online-Informationen
und Meldebogen).
Rhesus-D-Bestimmung bei Blutpräparaten
Für die Rhesus-D-Bestimmung bei Blutpräparaten
(Blutspendern) muß eine ergänzende Diagnostik durchgeführt
werden. Nur bei Blutpräparaten müssen auch äußerst
schwach ausgeprägte Rhesus-D-Antigene und partielle Rhesus-D-Antigene,
unter anderem Rhesus-D-Kategorien, erfaßt werden. Dies betrifft jedoch
ausschließlich Blutspendezentralen und transfusionsmedizinische Institute,
die eine Herstellungserlaubnis der zuständigen Regierungspräsidien
besitzen.
Diskrepanzen zwischen der Rhesus-D-Bestimmung als Patient
bzw. als Blutspender treten nur selten auf (< 0,1 %), wie Untersuchungen
ergeben haben [2]. Solche seltenen Diskrepanzen können
den transfundierten Patienten nie gefährden, da eine falsch-negative
Rhesus-D-Bestimmung beim Patienten immer eine Rhesus-D-negative Transfusion
indiziert. Dieses Vorgehen schließt auf jeden Fall eine Immunisierung
gegen das Rhesus-D-Antigen aus.
Nur bei allogenen Blutspendern muß bei der Erstbestimmung
ein Antiglobulintest durchgeführt werden, wenn die beiden Testansätze
mit IgM anti-D negativ sind. Dabei sollen oligoklonale anti-D Reagenzien
(Mischungen aus mehreren monoklonalen IgG und gegebenenfalls monoklonalen
IgM anti-D) verwendet werden. Ersatzweise können noch polyklonale
anti-D eingesetzt werden. Fällt der indirekte Antiglobulintest mit
diesen Seren positiv aus, gilt das Blutpräparat nach den Richtlinien
als Rhesus-D-positiv (Antigen D schwach ausgeprägt = weak D positiv
oder Dweak positiv).
Kennzeichnung
von Erythrozytenpräparaten
Entsprechend den klinischen Anforderungen ist ausschlaggebend,
ob das Erythrozytenpräparat Rh pos. oder Rh neg. ist. Ein schwach
ausgeprägtes Antigen D muß wie Rh pos. behandelt werden (Abbildung
1);
eine explizite Deklarierung des Präparates (zum
Beispiel weak D) bietet kaum Vorteile für die Labororganisation und
klinische Versorgung. Deswegen ist es sinnvoll - wie im Beispiel 4 der
Abbildung 1 gezeigt -, das Präparat als Rh pos. zu kennzeichnen und
die für den klinischen Anwender meist irrelevante Aussage zur Ausprägung
des Antigens D als Nebenbefund anzugeben. Alle partiellen Rhesus-D-Antigene
müssen ebenfalls als Rh pos. gekennzeichnet werden. Eine Angabe wie
D Kategorie VI etc. auf dem Blutpräparat ist nicht erforderlich, da
bisher keine Einschränkungen der klinischen Anwendbarkeit festgestellt
wurden. Das Vorgehen gilt entsprechend bei Thrombozytenpräparaten.
Bei Plasmapräparaten ist eine Deklarierung des Rhesusfaktors nicht
vorgeschrieben.
Abbildung 1. Beschriftung von Erythrozytenpräparaten.
Beispiel 1 zeigt die typische Beschriftung für ein Rhesus-D-positives Präparat (CcD.Ee) und Beispiel 2 für ein Rhesus-D-negatives
Präparat (ccddee). Auch Rhesus-D-negative Präparate mit großen
Buchstaben (Beispiel 3), hier Antigen E positiv (ccddEe), werden nach
den neuen Richtlinien für Rhesus negative Empfänger (ccddee)
verwendet. Beispiel 4 zeigt ein Rhesus-D-positives Präparat (ccD.Ee),
dessen Antigen D schwach ausgeprägt ist. Die Fallbeispiele 1 - 3 sind
Blutgruppe A und Antigen K negativ (Kell neg: kk). Beispiel 4 ist Blutgruppe
A und Antigen K positiv (Kell pos: Kk oder KK).
Rhesus-D-positives Präparat (CcD.Ee) und Beispiel 2 für ein Rhesus-D-negatives
Präparat (ccddee). Auch Rhesus-D-negative Präparate mit großen
Buchstaben (Beispiel 3), hier Antigen E positiv (ccddEe), werden nach
den neuen Richtlinien für Rhesus negative Empfänger (ccddee)
verwendet. Beispiel 4 zeigt ein Rhesus-D-positives Präparat (ccD.Ee),
dessen Antigen D schwach ausgeprägt ist. Die Fallbeispiele 1 - 3 sind
Blutgruppe A und Antigen K negativ (Kell neg: kk). Beispiel 4 ist Blutgruppe
A und Antigen K positiv (Kell pos: Kk oder KK).
Molekularbiologie der
Rhesusgene RHD und RHCE
Die Klärung des Protein- und Genpolymorphismus macht
schnelle Fortschritte [12, 13]. Alle
Antigene der Rhesus-Blutgruppe werden durch zwei benachbarte eng verwandte
(homologe) Gene, RHD und RHCE, gebildet. In der deutschen Bevölkerung
ist der Rhesus negative Phänotyp fast immer auf ein vollständiges
Fehlen des RHD-Gens zurückzuführen. Die Beschreibung der molekularen
Vielfalt beider Rhesus-Gene in der deutschen Population ist Vorraussetzung,
um eine sichere aber auch kosteneffiziente Strategie zur Rhesus-D-Bestimmung
mittels PCR zu etablieren. Eine solche Rhesus-D-Genotypisierung hat zum
Beispiel für die Pränataldiagnostik große Bedeutung [14].
Die dreidimensionale Struktur der Rhesus-Proteine ist
noch nicht bekannt. Erste Modelle zur Proteinkonfiguration sind entwickelt
worden (Abbildung 2). Das Antigen einer D Kategorie VI unterscheidet sich
vom normalen Rhesus-D-Antigen im extrazellären Anteil lediglich durch
drei von sieben polymorphen Aminosäuren. Wird ein Träger der
D Kategorie VI Rhesus positiv transfundiert, findet häufig eine Immunisierung
gegen diese Teile des Rhesus-D-Proteins statt, die der Transfusionsempfänger
selber nicht besitzt.
 Abbildung
2. Schematische Darstellung des Antigens D auf der Erythrozytenoberfläche.
Das normale RhD-Protein ist dargestellt (links). Jede Kugel symbolisiert
eine Aminosäure. Insgesamt sind sechs extrazelluläre Ketten von
Aminosäuren (Schlaufen) zu erkennen (hellgelb und hellgrau). Die
transmembranären Proteinanteile sind rötlich dargestellt. Das
RhD-Protein unterscheidet sich vom RhCE-Protein (hier nicht dargestellt)
lediglich in sieben extrazellulären Aminosäuren (gelb). Alle
anderen extrazellulären Aminosäuren (hellgelb und hellblau) sind
identisch zwischen dem RhD- und RhCE-Protein.
Abbildung
2. Schematische Darstellung des Antigens D auf der Erythrozytenoberfläche.
Das normale RhD-Protein ist dargestellt (links). Jede Kugel symbolisiert
eine Aminosäure. Insgesamt sind sechs extrazelluläre Ketten von
Aminosäuren (Schlaufen) zu erkennen (hellgelb und hellgrau). Die
transmembranären Proteinanteile sind rötlich dargestellt. Das
RhD-Protein unterscheidet sich vom RhCE-Protein (hier nicht dargestellt)
lediglich in sieben extrazellulären Aminosäuren (gelb). Alle
anderen extrazellulären Aminosäuren (hellgelb und hellblau) sind
identisch zwischen dem RhD- und RhCE-Protein.
Beim DVI-Protein (rechts) haben zwei Schlaufen statt
der RhD-spezifischen Aminosäuresequenz die RhCE-spezifische Aminosäuresequenz
(hellblau). Die extrazellulären Anteile des DVI-Proteins unterscheiden
sich also vom normalen RhD-Protein nur durch drei Aminosäuren (blau).
Weitere transmembranär und intrazellulär gelegene Unterschiede
können allerdings auch Einfluß auf die Proteinkonfiguration
nehmen und sind hier aus Gründen der Vereinfachung nicht dargestellt.
Ein Transfusionsempfänger mit dem Phänotyp
DVI kann einen anti D-Antikörper (blauer Pfeil) gegen die Anteile
des normalen Antigen D (gelb) bilden, die sein DVI Protein nicht aufweist,
weil sie durch RhCE-spezifische Anteile (hellblau und blau) ersetzt sind.
Gegen diese Teile des RhD-Proteins sind auch die monoklonalen IgM anti-D
gerichtet, die für die Typisierung von Transfusionsempfängern
benutzt werden. Da das DVI-Protein diese Anteile nicht besitzt, können
diese monoklonalen IgM anti-D nicht an das DVI-Protein binden und reagieren
serologisch negativ.
Für die D Kategorie VI waren bisher
zwei molekulare Ursachen bekannt (Typ I und Typ II). Beide Formen
weisen eine stark verminderte Anzahl von Rhesus-D-Proteinen in der Erythrozytenmembran
auf.Neuerdings wurde ein DVI Typ III beschrieben, dessen Erythrozyten eine
normale Anzahl von Rhesus-D-Proteinen tragen [15]. Trotz
der unterschiedlichen molekularen Struktur dieser drei Typen sind die extrazellulären
Anteile entsprechend dem Modell in Abbildung 2 kaum verschieden, was das
identische serologische Reaktionsmuster aller drei Typen erklärt.
Als Ursache schwach ausgeprägter Rhesus-D-Antigene findet sich ein
großer Genpolymorphismus [16], was bei der Genotypisierung
zu falsch-negativen oder falsch-positiven Ergebnissen führen kann.
Weiterhin ist die Genotypisierung mittels PCR [17] grundsätzlich
erschwert durch sporadische nicht-funktionale Allele [18].
Es gibt bereits Anhaltspunkte dafür, daß dies auch die pränatale
Rhesus-D-Genotypisierung komplizieren kann [16]. Natürliche
Hybridgene sind im Rhesus-Genlocus häufig. Die Charakterisierung der
molekularen Ursache partieller Rhesus-D-Antigene kann zum Verständnis
von Rekombinationsmechanismen beitragen, die zwischen den oft vorkommenden
benachbarten homologen Genen auftreten.
Ausblick
Monoklonale Antiseren in der Blutgruppenserologie sind
ein weiteres Beispiel wie biotechnologischer Fortschritt die Genauigkeit
in der Diagnostik und somit die Sicherheit in der Patientenversorgung erhöht.
Dies wird bei der Rhesus-D-Bestimmung erreicht, während die Gesamtkosten
dieser Diagnostik für das Gesundheitswesen vermindert werden. Die
Förderung der wissenschaftlichen Forschung über monoklonale antierythrozytäre
Antikörper hat im Ausland einen wesentlich höheren Stellenwert
inne. Es ist zu erwarten, daß der volkswirtschaftliche Nutzen dieser
Biotechnik, die zumindest für das nächste Jahrzehnt in der Blutgruppenserologie
bestimmend sein wird, dort in noch größerem Umfang zum Tragen
kommt. Die Genotypisierung wird die Bedeutung der monoklonalen Antikörper
als Schlüsseltechnologie eines Tages übertreffen. Die Transfusionsmedizin
kann zur Etablierung der Genotypisierung einen wesentlichen Beitrag leisten,
wenn es gelingt, die umfangreichen Datenbasen zu Blutgruppen-Phänotypen
hierfür wissenschaftlich zu nutzen.
Literatur
Hinweis:
Klicken Sie auf die Zitatnummer, um an eine repräsentative Textstelle
zu wechseln.
Klicken Sie die markierte Literaturstelle an, um den Medline-Eintrag
mit Abstrakt anzuschauen.
1
|
Wissenschaftlicher Beirat der Bundesärztekammer:
Richtlinien zur Blutgruppenbestimmung und Bluttransfusion ( Hämotherapie).
Kapitel 2.5.5: Bestimmung des Rh-Merkmals D. Deutscher Ärzteverlag,
Köln 1996. |
2
|
Wagner FF, Kasulke D, Kerowgan M, Flegel WA: Frequencies
of blood groups ABO, Rhesus, D category VI, Kell, and of clinically relevant
high-frequency antigens in South-Western Germany. Infusionsther
Transfusionsmed 1995;22:285-290. |
3
|
Endres W, Flegel WA, Helmbold W, Kasulke D, Montag-Lessing
T, Poschmann A, Sonneborn HH: Überlegungen zum Vorgehen bei der Bestimmung
der D-Eigenschaft. Infusionsther Transfusionsmed 1996;23:172-175. |
| 4 |
Bundesärztekammer: Richtlinien der Bundesärztekammer
zur Qualitätssicherung in der Immunhämatologie. Deutsches Ärzteblatt
1992;89 |
5
|
Agre PC, Davies DM, Issitt PD, Lamy BM, Schmidt PJ, Treacy
M, Vengelen-Tyler V: A proposal to standardize terminology for weak D antigen
(Leserbrief). Transfusion
1992;32:86-87. |
| 6 |
Flegel WA, Wagner FF: The frequency of RHD protein variants
in Caucasians (Abstrakt). Transfus Clin Biol 1996;3:10s. |
7
|
Jones JW, Lloyd-Evans P, Kumpel BM: Quantitation of Rh
D antigen sites on weak D and D variant red cells by flow cytometry. Vox
Sang 1996;71:176-183. |
8
|
Flegel WA, Wagner FF: RHD epitope density profiles of
RHD variant red cells analyzed by flow cytometry. Transfus
Clin Biol 1996;6:429-431. |
9
|
Avent ND, Jones JW, Liu W, Scott M, Voak D, Flegel WA,
Wagner FF, Green C: Molecular basis of the D variant phenotypes DNU and
DII allows localization of critical amino acids required for expression
of Rh D epitops epD3, 4 and 9 to the sixth external domain of the Rh D
protein. Br
J Haematol 1997;97:366-371. |
10
|
Jones J, Scott ML, Voak D: Monoclonal anti-D specificity
and Rh D structure: criteria for selection of monoclonal anti-D reagents
for routine typing of patients and donors. Transfus
Med 1995;5,171-184. |
11
|
Vorstand und wissenschaftlicher Beirat der Bundesärztekammer:
Leitlinien zur Therapie mit Blutkomponenten und Plasmaderivaten. Deutscher
Ärzteverlag, Köln, 1995; Seiten 18-19. |
12
|
Tippett P, Lomas-Francis C, Wallace M: The Rh antigen
D: partial D antigens and associated low incidence antigens. Vox
Sang 1996;70:123-131. |
13
|
Neumeister B, Flegel WA, Northoff H: Biochemie der Rh-Blutgruppenantigene
und ihre Bestimmung mittels monoklonaler Testseren. Clin Lab 1996;42:279-283. |
14
|
Bennett PR, Le Van Kim C, Colin Y, Warwick RM, Cherif-Zahar
B, Fisk NM, Cartron JP: Prenatal determination of fetal RhD type by DNA
amplification: N
Engl J Med 1993;329:607-610. |
15
|
Wagner FF, Gassner C, Müller TH, Schönitzer
D, Schunter F, Flegel WA: Three molecular structures cause Rhesus-D category
VI phenotypes with distinct immunohematologic features. Blood 1998;93 (im
Druck) |
16
|
Avent ND, Martin PG, Armstrong-Fisher SS, Liu W, Finning
KM, Maddocks D, Urbaniak SJ: Evidence of genetic diversity underlying Rh
D negative, weak D (Du) and partial D phenotypes as determined by multiplex
PCR analysis of the RHD gene. Blood
1997;89:2568-2577. |
17
|
Gassner C, Schmarda A, Kilga-Nogler S, Jenny-Feldkircher
B, Rainer E, Müller TH, Wagner FF, Flegel WA, Schönitzer D: RHD/CE
typing by polymerase chain reaction using sequence-specific primers.Transfusion
1997;37:1020-1026. |
18
|
Wagner FF, Flegel WA: Polymorphism of the h allele and
the population frequency of sporadic non-functional alleles. Transfusion
1997;37:284-290. |
Zur Inhaltsübersicht
Homepage Abteilung
Blutgruppenserologie und Immunhämatologie, DRK-Blutspendezentrale
Ulm, D-89081 Ulm, Germany
Sponsored by the DRK-Blutspendedienst Baden-Württemberg
last modified 18 Feb 1998
 gestaltet.
Die Autoren bedanken sich beim Umschau Zeitschriftenverlag
und der Chefredakteurin Dr. S. Päuser
für die freundliche Genehmigung zur elektronischen Wiedergabe des
Zeitschriftenbeitrags. Auszüge aus dem zugrundeliegenden Manuskript
wurden 1997 auch als Verlautbarung des Berufsverbandes Deutscher Transfusionsmediziner
unter dem Titel Stand der Rhesus-D Bestimmung beim Transfusionsempfänger
veröffentlicht.
gestaltet.
Die Autoren bedanken sich beim Umschau Zeitschriftenverlag
und der Chefredakteurin Dr. S. Päuser
für die freundliche Genehmigung zur elektronischen Wiedergabe des
Zeitschriftenbeitrags. Auszüge aus dem zugrundeliegenden Manuskript
wurden 1997 auch als Verlautbarung des Berufsverbandes Deutscher Transfusionsmediziner
unter dem Titel Stand der Rhesus-D Bestimmung beim Transfusionsempfänger
veröffentlicht.



 Abbildung
2. Schematische Darstellung des Antigens D auf der Erythrozytenoberfläche.
Das normale RhD-Protein ist dargestellt (links). Jede Kugel symbolisiert
eine Aminosäure. Insgesamt sind sechs extrazelluläre Ketten von
Aminosäuren (Schlaufen) zu erkennen (hellgelb und hellgrau). Die
transmembranären Proteinanteile sind rötlich dargestellt. Das
RhD-Protein unterscheidet sich vom RhCE-Protein (hier nicht dargestellt)
lediglich in sieben extrazellulären Aminosäuren (gelb). Alle
anderen extrazellulären Aminosäuren (hellgelb und hellblau) sind
identisch zwischen dem RhD- und RhCE-Protein.
Abbildung
2. Schematische Darstellung des Antigens D auf der Erythrozytenoberfläche.
Das normale RhD-Protein ist dargestellt (links). Jede Kugel symbolisiert
eine Aminosäure. Insgesamt sind sechs extrazelluläre Ketten von
Aminosäuren (Schlaufen) zu erkennen (hellgelb und hellgrau). Die
transmembranären Proteinanteile sind rötlich dargestellt. Das
RhD-Protein unterscheidet sich vom RhCE-Protein (hier nicht dargestellt)
lediglich in sieben extrazellulären Aminosäuren (gelb). Alle
anderen extrazellulären Aminosäuren (hellgelb und hellblau) sind
identisch zwischen dem RhD- und RhCE-Protein.